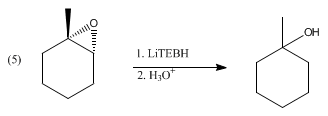Trietilboroidruro di litio
Il trietilboroidruro di litio è un composto organoboro con la formula LiEt3BH. Comunemente indicato come LiTEBH o superidruro, è un potente agente riducente utilizzato nella chimica organometallica e organica. È un liquido incolore o bianco, ma viene generalmente commercializzato e utilizzato come soluzione in THF.[1] Il relativo agente riducente, il trietilboroidruro di sodio, è disponibile in commercio come soluzioni di toluene.
Il trietilboroidruro di litio è un agente riducente più forte del boroidruro di litio e del tetraidroalluminato di litio.
Preparazione
Il trietilboroidruro di litio è preparato dalla reazione di idruro di litio (LiH) e trietilborano (Et3B) in tetraidrofurano (THF):
Le sue soluzioni THF sono stabili indefinitamente in assenza di umidità e aria.
Reazioni
Gli alogenuri alchilici sono ridotti ad alcani dal trietilboroidruro di litio[2][3][1].
Il trietilboroidruro di litio riduce un'ampia gamma di gruppi funzionali, reazione che è tuttavia comune anche a molti altri reagenti idruro. Il trietilboroidruro di litio è però riservato a substrati difficili, come carbonili stericamente impediti, come illustrato dalla riduzione del 2,2,4,4-tetrametil-3-pentanone. In aggiunta riduce le anidridi acide a alcol e acido carbossibilico, ma non ai corrispondenti dioli. Invece i lattoni si riducono a dioli. Gli α,β-enoni subiscono un'addizione 1,4 per dare enolati di litio. I disolfuri si riducono a tioli (tramite tiolati). Il trietilboroidruro di litio deprotona gli acidi carbossilici, ma non riduce i risultanti carbossilati di litio. Per ragioni simili, gli epossidi subiscono l'apertura dell'anello dopo il trattamento con LiBHEt3 per dare l'alcol. Con epossidi asimmetrici, la reazione può procedere con elevata regioselettività e stereoselettività, favorendo l'attacco nella posizione meno impedita: [1]
Gli acetali e i chetali non vengono ridotti dal trietilboroidruro di litio. Può essere utilizzato nella scissione riduttiva di mesilati e tosilati[4]. Il trietilboroidruro di litio può deproteggere selettivamente i gruppi N-acile terziari senza influenzare la funzionalità dell'ammide secondaria[5]. Ha anche dimostrato di ridurre gli esteri aromatici agli alcoli corrispondenti come mostrato nelle reazioni 6 e 7:
Il trietilboroidruro di litio riduce anche la piridina e le isochinoline rispettivamente in piperidine e tetraidroisochinoline[6].
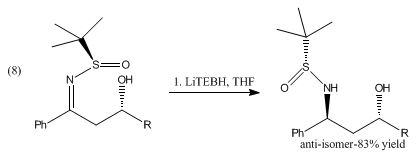
La riduzione delle β-idrossisolfinil immine con catecolborano e il trietilboroidruro di litio produce gli anti-1,3-amminoalcoli mostrati in (8) [7].
Precauzioni
Il trietilboroidruro di litio reagisce esotermicamente, potenzialmente anche in modo violento, con acqua, alcoli e acidi, liberando idrogeno e trietilborano piroforico[1].